Оксалат натрия — химическое соединение, соль натрия и щавелевой кислоты с формулой Na2C2O4, бесцветные кристаллы, слабо растворяется в воде.
Рассмотрим получение двумя способами:
1) из H2C2O4 (Щавелевая кислота) и NaOH (Гидроксид натрия, другие названия - каустическая сода, каустик, едкий натр, едкая щёлочь)
2) из H2C2O4 (Щавелевая кислота) и NaHCO3 (пищевой соды он же гидрокарбонат натрия)
ПЕРВЫЙ СПОСОБ:
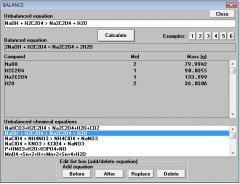
2NaOH + H2C2O4 = Na2C2O4 + 2H2O
NaOH = 80 гр
Щавелевой кислоты = 90 гр.
теоретический выход оксалата = 134 гр.
1) Растворяем 80 гр NaOH в 80 гр. холодной воды
2) Растворяем = 90 гр. Щавелевой кислоты в 100 гр. горячей воды
Реакцию экзотермическая (выделение теплоты) и очень бурная, поэтому проводить реакцию в такой колбе,
NaOH растворенный в воде вливается порционно в раствор Щавелевой кислоты
Температура поднимается до 100 гр. С, требуется охлаждение (кастрюля с водой и льдом)
выпадает мелкий белый осадок, по окончанию вливания - перемешиваем взбалтываем и охлаждаем.
далее :
поскольку реакция протекает не в идеальных условиях, то либо выравниваем pH либо сразу промываем наш раствор,
- смотрим на pH раствора, и выравниваем до нейтральной реакции ( добавляем NaOH или H2C2O4 )
пока pH не станет нейтральным
- фильтруем осадок на воронке брюхнера
- промываем и сушим
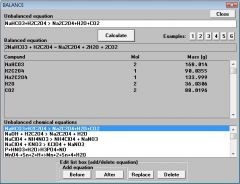
2NaHCO3 + H2C2O4 = Na2C2O4 + 2H2O + 2CO2
Соды = 168 гр.
Щавелевой кислоты = 90 гр.
теоретический выход оксалата = 134 гр.
в принципе тоже самое, только соду не надо полностью растворять в воде ( растворимость всего 9,59 г/100 мл)
Сообщение отредактировал megaplast: 18 February 2015 - 19:56